全国のインキュベーション施設

2025年12月10日
アクチュアライズ株式会社
大学発の研究成果を生かし、 角膜移植に代わる世界初の眼科治療を実現へ

眼の角膜の病気にかかると視力が低下し生活に支障をきたすにもかかわらず、これまでは角膜移植しか治療法がありませんでした。一方で、移植用の角膜はドナー不足により、患者の70人に1人しか移植を受けられないのが現状です。アクチュアライズは、同志社大学で培われた角膜内皮細胞の研究成果を生かし、角膜移植に代わる世界初の眼科治療の実現に挑みます。代表取締役社長である松岡靖史氏にそのインパクトについて伺いました。(2025年11月取材)
インタビュー
-
お話
-
アクチュアライズ株式会社
(同志社大学連携型起業家育成施設(D-egg)入居)
代表取締役社長 松岡 靖史氏
起業、会社のおいたち
会社設立の経緯をお聞かせください
人の眼の前面には角膜という透明な組織があり、その裏側にある角膜内皮の働きによって角膜の透明性が保たれています。角膜内皮が病気などで傷んでしまうと角膜が白く濁ってしまい、視力が下がってしまうのですが、治療法としてこれまでは角膜移植しかありませんでした。この角膜移植に必要なドナー角膜は世界的に不足しており、患者70人に対し1人の割合でしか受けられません。日本では、待機患者としてアイバンクに登録されているのは2000人程度ですが、潜在患者を含めると推定で2万人以上の患者が角膜移植を必要としている状況です。

当社の創業メンバーである同志社大学の小泉範子教授、奥村直毅教授は眼科専門医であり、角膜内皮疾患に対する薬物治療、再生治療の研究を行ってきました。その中で、基本的には再生しないと言われていた角膜内皮細胞の効率的な培養に成功し、さらにこの細胞を患者の眼に注射することで角膜移植の代わりになることを発見しました。いずれも世界初の成果と言えます。
角膜移植に代わる眼科治療の新たな道筋を見いだしたわけですね
自分たちで作り上げた価値あるものを患者に届けたい、そういった想いからこれらの研究成果を社会実装するため、2018年5月にアクチュアライズが設立されました。
事業の展開と現在
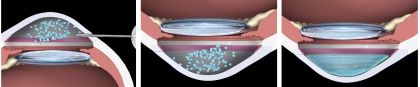
御社の技術が、なぜドナー角膜不足の問題を解決できるのでしょうか
私たちの技術により、アイバンクから提供を受けた一人のドナー角膜から50~100人分に移植できるように角膜内皮細胞を培養し増やすことができるようになりました。これで移植を必要としている患者の70人に1人にしかドナー角膜がないという問題を計算上、解決できることになります。
また、従来の角膜細胞の培養では、製造後48時間以内に使用しなければならないという制限がありましたが、私たちは特殊な方法により、培養した細胞を凍結保存できる製剤を開発することに成功しました。すでに3年間保存可能というデータも出てきています。これによって、一つの拠点で製造した細胞を世界中の病院に輸送し、必要な時に解凍して患者の眼に注射できる「Ready to Use(すぐに使える)」を実現できます。眼内への細胞の注射は10分で終わり、その後、患者には3時間ほどうつ伏せの姿勢になってもらい、重力を利用して角膜の裏側に細胞を集積させると角膜内皮が所定の場所に生着して再生します。
そのほかにどのような開発を進めていますか
「フックス角膜内皮ジストロフィ」という角膜内皮の病気を治療する点眼薬を開発しています。この病気は欧米人の40歳以上の4%がかかるとされており、進行するとまぶしさや視力の低下を感じるようになります。これまで治療薬がなかったために視力が低下して生活が不自由になってから角膜移植が行われていました。世界中で行われる角膜移植の原因の第1位にもなっており、治療薬の開発が強く期待されていました。
同志社大学生命医科学部では、この病気の原因を解明する一環として、培養した角膜内皮細胞から疾患モデル細胞」を作成し、治療薬となり得る薬を調べる薬物スクリーニングを行いました。その結果、「シロリムス」という薬剤に病気の進行を抑える効果があることを突き止め、治療薬用途の特許出願を行いました。私たちは同志社大学からこの特許についての独占的実施権を取得し、治療薬として開発を進めています。2021年11月には、参天製薬とフックス角膜内皮ジストロフィを対象としたシロリムス点眼薬の臨床試験を開始するための共同開発契約を締結しています。2022年には米国、フランス、インドで臨床試験が開始されました。臨床試験で安全性、有効性が証明されたら、世界初のフックス角膜内皮ジストロフィの治療薬として発売されることになります。
そしてこれから
今後の展開について教えてください
角膜内皮再生用の凍結製剤、シロリムス点眼薬のそれぞれの製造販売の承認に向けて、臨床試験を進めていきます。
凍結製剤については、2024年9月に日本で有効性と安全性を調べる第II相試験を開始し、2025年11月に最終症例の評価を終了しました。現在、第Ⅱ相試験の結果の解析を進めており、この結果を基に2026年には比較的多くの症例を用いて薬効を検証する第Ⅲ相試験の治験届を提出する予定です。第Ⅲ相試験の結果が想定通りであれば、2030年頃に承認されることを期待しています。一方、中国での凍結製剤の開発については、既に中国Arctic Vision社と独占的ライセンス契約を締結しています。Arctic Visionは当社の協力の下、2026年初頭から臨床試験を開始する予定であり、中国で承認を得るまでに6年ぐらいかかると見ています。
インキュベーションの利用
入居のきっかけ、入居してよかったこと
起業後に出資を受けた段階で、管理機能のある本社をどこかに置く必要があり、同志社大学との相談の中でこの施設を紹介していただきました。やはり研究現場のある同志社大学の近くにあるというのがメリットとして大きいですね。今は事務室として使っていますが、いずれは研究室もこちらに移転したいと思っており、そういった設備も整っているというのが決め手となりました。施設のスタッフから色々とサポートしていただき、困った時も的確な情報をいただけるので助かっています。
今後インキュベーション施設を利用する方へのメッセージ
実は中小基盤整備機構の施設は、ほかにも利用したことがあります。そこも含めて共通しているのですが、規模的にもちょうど良く、会議室などユーティリティも充実しているのに費用がそれほどかからない、スタートアップにとってとても使いやすい施設だと思います。
会社情報
会社名 |
|
|---|---|
代表取締役社長 |
松岡 靖史 |
所在地 |
京都府京田辺市興戸地蔵谷1番地 同志社大学連携型起業家育成施設(D-egg)314号室 |
事業概要 |
角膜内皮疾患に対する再生医療用細胞製品と点眼治療薬の開発・製品化 |
会社略歴
2018年5月 |
アクチュアライズ株式会社を設立 |
|---|---|
2019年10月 |
合計約4.7億円の第三者割当増資を実施 |
2021年5月 |
中国Arctic Vision社に角膜内皮再生医療製品候補(AE101)をライセンス |
2021年11月 |
参天製薬とフックス角膜内皮ジストロフィを対象とした共同開発契約 |
2022年5月 |
フックス角膜内皮ジストロフィを対象とした第Ⅱ相臨床試験を米国で開始 |
2022年8月 |
角膜内皮の再生医療製品候補(AE101)の製造をJ-TECで開始 |
2024年9月 |
再生医療用細胞製品の国内第Ⅱ相臨床試験における第一例目の移植実施 |
2025年11月 |
再生医療等製品の国内第Ⅱ相試験の最終症例の観察を終了 |
担当マネージャーからのコメント

アクチュアライズは、同志社大学ティッシュエンジニアリング研究室と連携して角膜内皮障害の新たな治療法の開発に取り組んでいます。主要な開発品の角膜内皮障害治療点眼薬と角膜内皮再生医療用細胞製品をより早く提供するため、国内バイオベンチャー企業との共同開発や臨床試験の実施、製薬会社と共同での海外臨床試験の実施、再生医療用細胞の生産委託先との連携、海外企業へのライセンシングと臨床試験支援など、経営者や先生方のネットワークを活用して共創による社会実装を進めています。
2024年からは再生医療用細胞製品の国内での第Ⅱ相臨床試験が始まり、D-eggにある本社では情報管理システムの整備など、新たな取り組みも積極的に進めています。当社の熱意と企業連携により、眼科医療の「アンメット・メディカル・ニーズ(いまだ満たされない医療ニーズ)」の解決策が早く患者さんに届けられることを期待しています。
